Évolution spontanée d'un système chimique
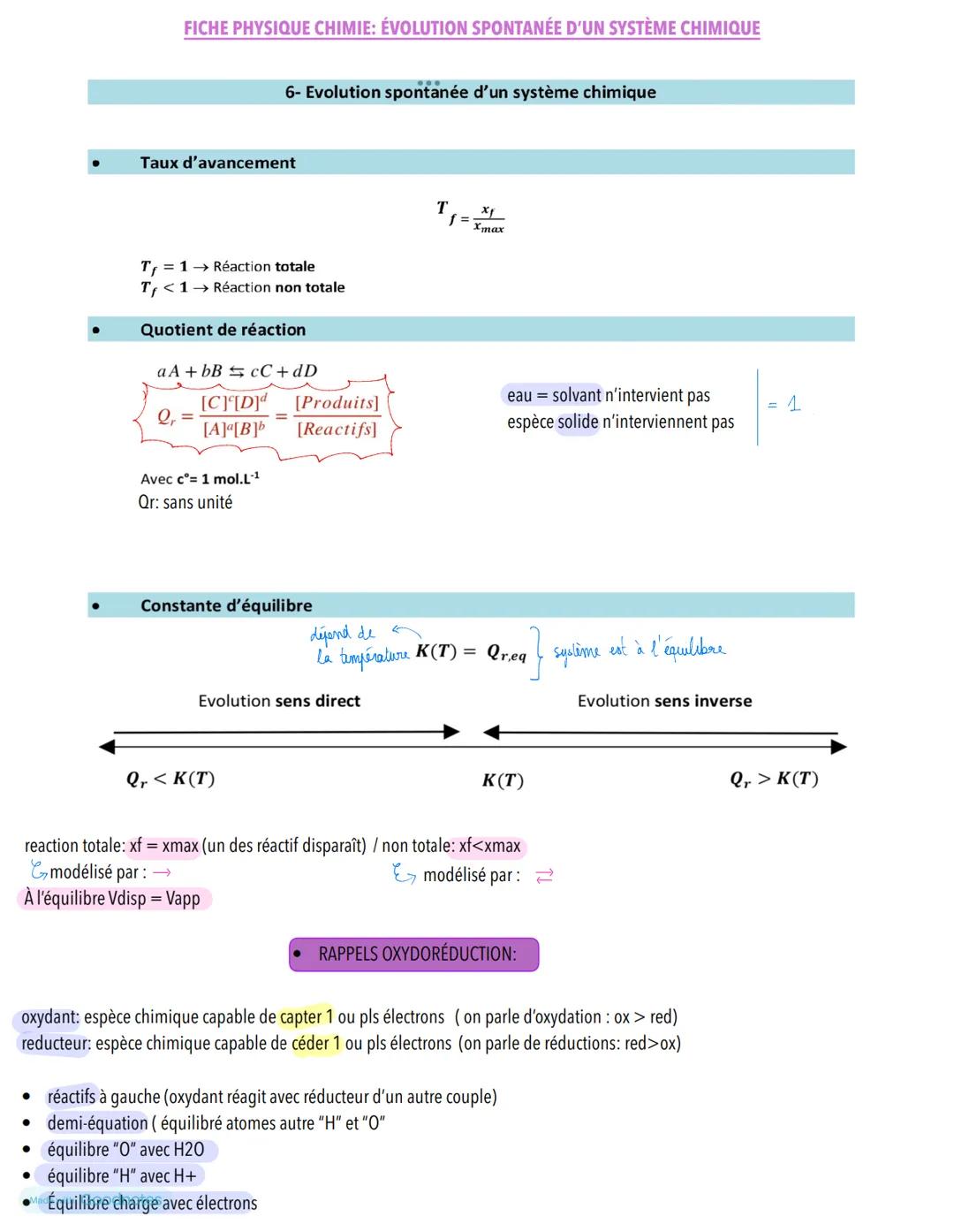
Le taux d'avancement te dit si ta réaction va jusqu'au bout ou s'arrête en cours de route. Avec la formule Tf = xf/xmax, tu obtiens un chiffre entre 0 et 1.
Si Tf = 1, c'est jackpot : ta réaction est totale et un des réactifs disparaît complètement. Si Tf < 1, ta réaction est non totale et s'arrête avant la fin, créant un équilibre.
Le quotient de réaction Qr compare les concentrations des produits et des réactifs à un moment donné. Pour aA + bB ⇌ cC + dD, tu calcules Qr = C^cD^d / A^aB^b. Attention : l'eau (solvant) et les solides ne comptent pas dans le calcul !
Astuce pratique : Retiens que Qr n'a pas d'unité grâce à la concentration de référence c° = 1 mol.L⁻¹
La constante d'équilibre K(T) dépend uniquement de la température. Quand Qr = K(T), ton système est à l'équilibre avec des vitesses de disparition et d'apparition égales. Si Qr < K(T), la réaction évolue dans le sens direct, et si Qr > K(T), elle recule.