La quantité de matièreest un concept clé en chimie... Affiche plus
Inscris-toi pour voir le contenuC'est gratuit!
Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Knowunity AI
Matières
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Affiche tous les sujets
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Affiche tous les sujets
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Affiche tous les sujets
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Affiche tous les sujets
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Affiche tous les sujets
159
•
Mis à jour Apr 13, 2026
•
Zélie
@zlie_mart
La quantité de matièreest un concept clé en chimie... Affiche plus



Imagine que tu veuilles compter les grains de sable sur une plage - impossible ! En chimie, c'est pareil avec les atomes, alors on utilise la mole comme unité de comptage.
Une mole contient toujours le même nombre d'entités : 6,02 × 10²³ (c'est la constante d'Avogadro). Pour calculer combien tu as de moles, tu utilises n = N/NA pour les solides ou n = m/M où M est la masse molaire.
Pour les gaz, c'est encore plus simple ! À 20°C, une mole de n'importe quel gaz occupe 24,0 L. Donc n = V/Vm et tu as ton résultat.
Astuce : La masse molaire se lit directement sur le tableau périodique - pratique non ?

Tu veux faire une solution ? Deux techniques principales : la dissolution (mélanger un soluté dans un solvant) et la dilution (rendre une solution moins concentrée).
Pour une dissolution, tu calcules d'abord n = C × V, puis m = n × M pour savoir combien peser. Simple ! Pour une dilution, retiens cette formule magique : Co × Vo = C₁ × V₁.
Le facteur de dilution te dit combien de fois tu dilues. Si F = 10, ta concentration finale sera 10 fois plus faible. Tu calcules le volume à prélever avec Vmère = Vfille/F.
Point clé : Lors d'une dilution, la quantité de soluté reste constante - seul le volume change !
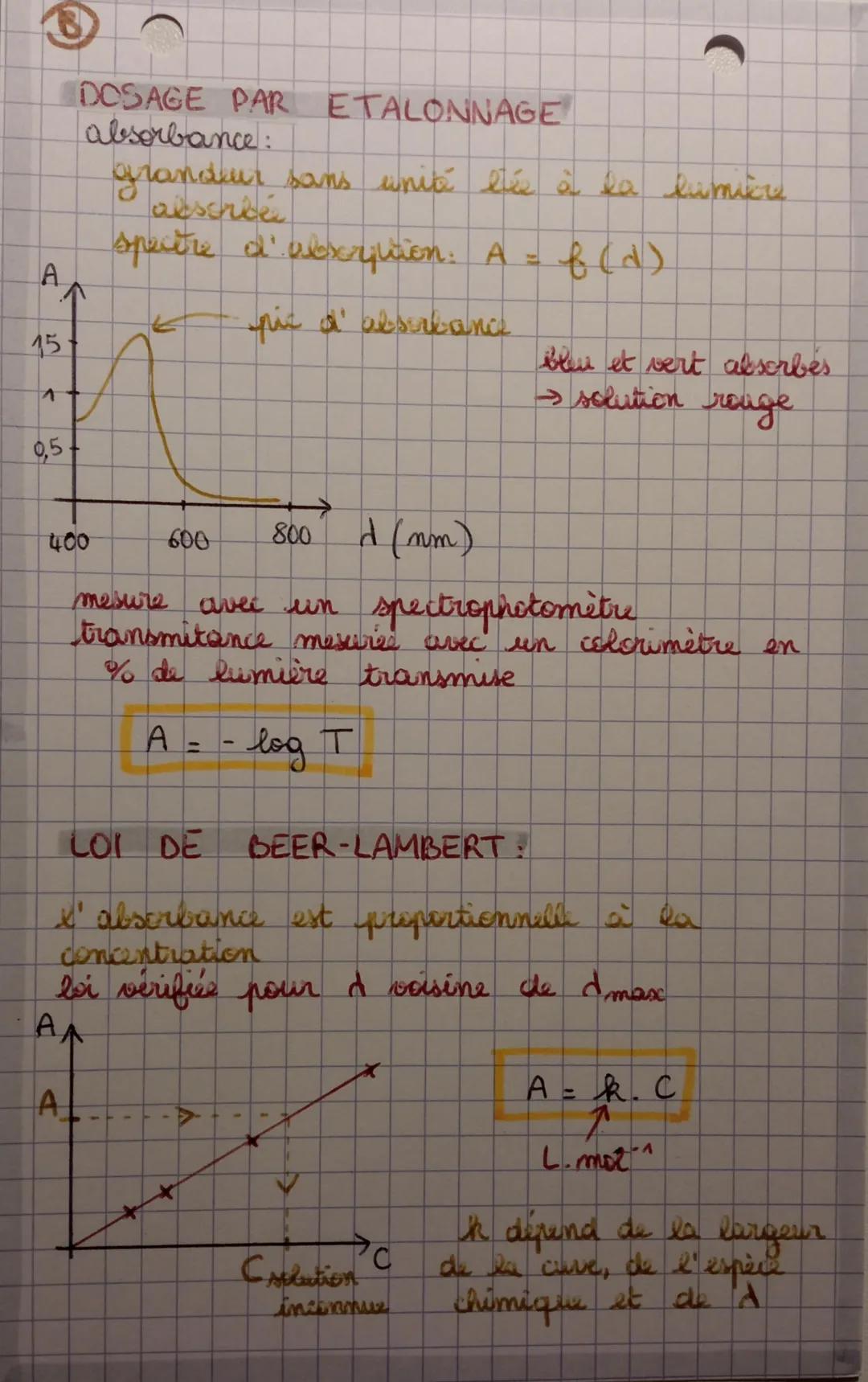
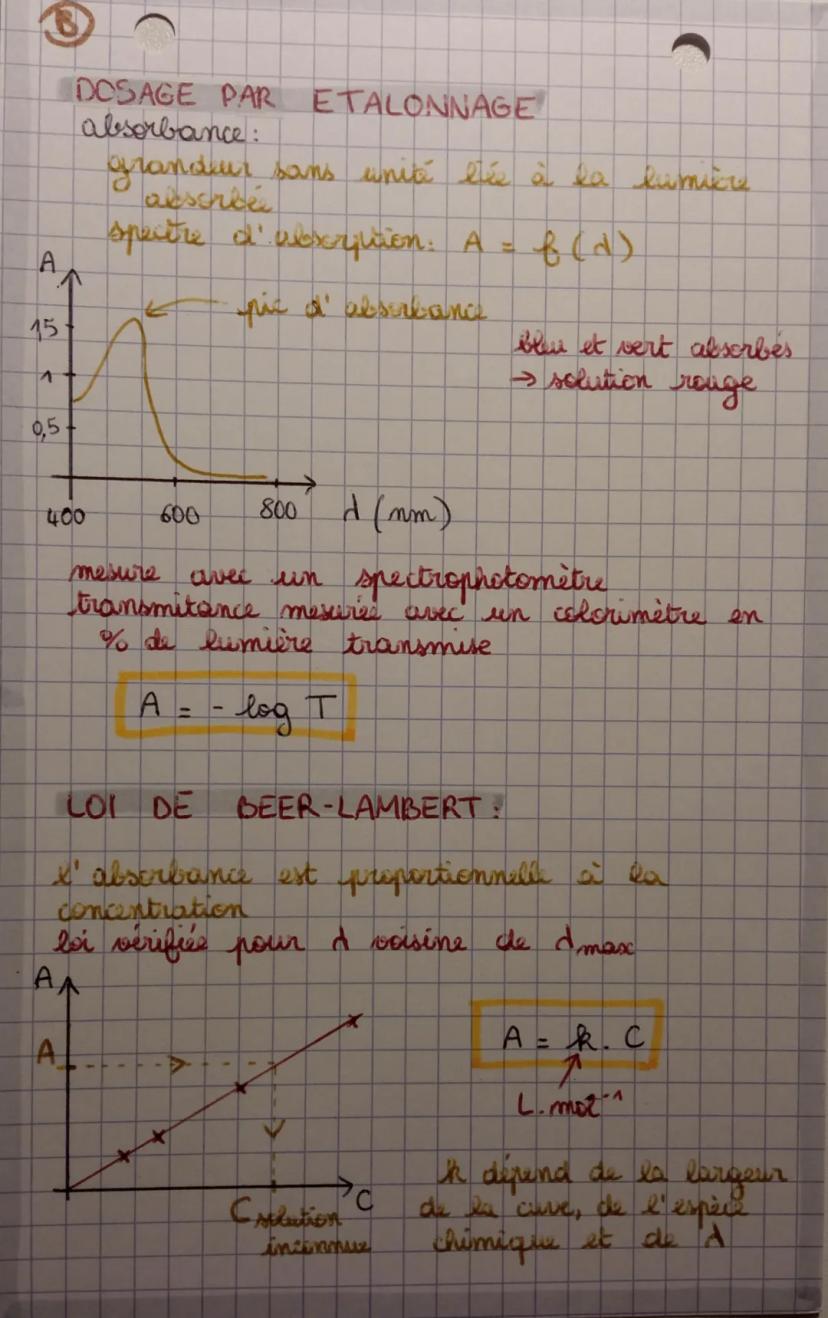
Le dosage par étalonnage utilise la lumière pour mesurer une concentration - génial non ? Chaque substance absorbe certaines couleurs et en laisse passer d'autres.
L'absorbance (notée A) mesure la lumière absorbée avec un spectrophotomètre. Plus la solution est concentrée, plus elle absorbe de lumière. La loi de Beer-Lambert dit que A = ε × l × C.
Cette relation linéaire entre absorbance et concentration te permet de créer une courbe d'étalonnage. Tu mesures l'absorbance de solutions connues, tu traces la droite, et hop ! Tu peux déterminer n'importe quelle concentration inconnue.
Conseil pratique : Travaille toujours près de λmax pour que la loi de Beer-Lambert soit bien vérifiée !
Notre compagnon IA est spécialement conçu pour répondre aux besoins des étudiants. Sur la base des millions d'éléments de contenu que nous avons sur la plateforme, nous pouvons fournir des réponses vraiment significatives et pertinentes aux étudiants. Mais il ne s'agit pas seulement de réponses, le compagnon a encore plus pour but de guider les élèves dans leurs défis d'apprentissage quotidiens, avec des plans d'étude personnalisés, des quiz ou des éléments de contenu dans le chat et une personnalisation à 100% basée sur les compétences et les développements de l'étudiant.
Tu peux télécharger l'application dans Google Play Store et dans l'App Store d'Apple.
Oui, tu as un accès entièrement gratuit à tous les contenus de l'appli, tu peux chatter ou suivre les créateurs à tout moment. De plus, nous proposons Knowunity Premium, qui te permet de réviser sans limites!
67
2
App Store
Google Play
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS
Zélie
@zlie_mart
La quantité de matièreest un concept clé en chimie qui te permet de compter les atomes et molécules, même si tu ne peux pas les voir ! Tu vas découvrir comment passer d'une masse à un nombre de moles,... Affiche plus

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Imagine que tu veuilles compter les grains de sable sur une plage - impossible ! En chimie, c'est pareil avec les atomes, alors on utilise la mole comme unité de comptage.
Une mole contient toujours le même nombre d'entités : 6,02 × 10²³ (c'est la constante d'Avogadro). Pour calculer combien tu as de moles, tu utilises n = N/NA pour les solides ou n = m/M où M est la masse molaire.
Pour les gaz, c'est encore plus simple ! À 20°C, une mole de n'importe quel gaz occupe 24,0 L. Donc n = V/Vm et tu as ton résultat.
Astuce : La masse molaire se lit directement sur le tableau périodique - pratique non ?

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Tu veux faire une solution ? Deux techniques principales : la dissolution (mélanger un soluté dans un solvant) et la dilution (rendre une solution moins concentrée).
Pour une dissolution, tu calcules d'abord n = C × V, puis m = n × M pour savoir combien peser. Simple ! Pour une dilution, retiens cette formule magique : Co × Vo = C₁ × V₁.
Le facteur de dilution te dit combien de fois tu dilues. Si F = 10, ta concentration finale sera 10 fois plus faible. Tu calcules le volume à prélever avec Vmère = Vfille/F.
Point clé : Lors d'une dilution, la quantité de soluté reste constante - seul le volume change !

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Le dosage par étalonnage utilise la lumière pour mesurer une concentration - génial non ? Chaque substance absorbe certaines couleurs et en laisse passer d'autres.
L'absorbance (notée A) mesure la lumière absorbée avec un spectrophotomètre. Plus la solution est concentrée, plus elle absorbe de lumière. La loi de Beer-Lambert dit que A = ε × l × C.
Cette relation linéaire entre absorbance et concentration te permet de créer une courbe d'étalonnage. Tu mesures l'absorbance de solutions connues, tu traces la droite, et hop ! Tu peux déterminer n'importe quelle concentration inconnue.
Conseil pratique : Travaille toujours près de λmax pour que la loi de Beer-Lambert soit bien vérifiée !
Notre compagnon IA est spécialement conçu pour répondre aux besoins des étudiants. Sur la base des millions d'éléments de contenu que nous avons sur la plateforme, nous pouvons fournir des réponses vraiment significatives et pertinentes aux étudiants. Mais il ne s'agit pas seulement de réponses, le compagnon a encore plus pour but de guider les élèves dans leurs défis d'apprentissage quotidiens, avec des plans d'étude personnalisés, des quiz ou des éléments de contenu dans le chat et une personnalisation à 100% basée sur les compétences et les développements de l'étudiant.
Tu peux télécharger l'application dans Google Play Store et dans l'App Store d'Apple.
Oui, tu as un accès entièrement gratuit à tous les contenus de l'appli, tu peux chatter ou suivre les créateurs à tout moment. De plus, nous proposons Knowunity Premium, qui te permet de réviser sans limites!
8
Outils Intelligents NOUVEAU
Transforme cette fiche en : ✓ 50+ Questions d'Entraînement ✓ Cartes Mémoire Interactives ✓ Examen blanc complet ✓ Plans de Dissertation
Explorez les principes du dosage spectrophotométrique, y compris le cercle chromatique, la loi de Beer-Lambert, et la relation entre absorbance et concentration. Ce document fournit des calculs pratiques et des exemples d'application pour le contrôle de qualité en chimie. Type : résumé.
Explorez les principes du contrôle qualité en chimie, notamment le dosage par étalonnage et la loi de Beer-Lambert. Ce document aborde l'absorbance des solutions, les techniques de spectroscopie UV-Vis, et les calculs de concentration. Idéal pour les étudiants en chimie souhaitant approfondir leur compréhension des méthodes d'analyse quantitative.
fiche avec 3 chapitres de SPE physique-chimie dans le thème 1 : Constitution et transformation de la matière et dans le thème 2 : Ondes et signaux
Explorez les principes du dosage spectrophotométrique pour déterminer la concentration d'une solution. Ce document couvre les concepts clés tels que l'absorbance, la dilution, la loi de Beer-Lambert, et les calculs de concentration molaire. Idéal pour les étudiants en première spécialité, il inclut des protocoles de dosage et des méthodes d'étalonnage.
Explorez les principes fondamentaux de la spectrophotométrie, y compris la loi de Beer-Lambert et la mesure de l'absorbance. Ce document présente des méthodes pour déterminer la concentration d'une espèce chimique en solution à l'aide d'un spectrophotomètre, en mettant l'accent sur les solutions colorées et incolores. Idéal pour les étudiants en chimie cherchant à comprendre les bases de l'ultraviolet-visible (UV-Vis) spectroscopy.
Bonnes révisions !
67
2
App Store
Google Play
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS