Salut ! On va explorer la qualité de l'eau, un... Affiche plus
Comprendre la qualité de l'eau







Solubilité et conductivité : les bases de la chimie de l'eau
Tu sais que l'eau du robinet conduit l'électricité ? C'est grâce aux ions dissous qu'elle contient ! L'eau pure (H₂O) est une molécule polaire : l'oxygène est légèrement négatif, les hydrogènes légèrement positifs.
Cette polarité permet à l'eau de dissoudre facilement les solides ioniques comme le sel de cuisine (NaCl). La solubilité te dit combien de grammes maximum tu peux dissoudre dans 1 L d'eau. Par exemple, le sel a une solubilité de 358,5 g/L à 25°C.
Quand un solide ionique se dissout, il libère ses ions dans l'eau : NaCl(s) → Na⁺(aq) + Cl⁻(aq). Ces ions bougent librement et permettent le passage du courant électrique.
💡 Astuce pratique : Plus une eau contient d'ions, mieux elle conduit l'électricité. C'est pourquoi l'eau distillée (sans ions) ne conduit pas du tout !
La conductivité se mesure avec un conductimètre en siemens par mètre . Elle dépend de la nature des ions, leur concentration, et la température de la solution.

Dosage par titrage conductimétrique : mesurer précisément les ions
Le titrage conductimétrique est ta technique de référence pour connaître la concentration exacte d'un ion dans l'eau. C'est comme une recette de cuisine chimique !
Le principe est simple : tu verses progressivement une solution titrante (concentration connue) dans ta solution titrée (concentration inconnue). À chaque ajout, tu mesures la conductivité avec ton conductimètre.
La courbe obtenue forme deux segments de droite qui se croisent au point d'équivalence. C'est le moment magique où tous tes ions ont réagi dans les bonnes proportions ! L'abscisse de ce point te donne le volume équivalent Veq.
💡 Formule clé : À l'équivalence, les réactifs respectent la stœchiométrie de l'équation de réaction.
Pour calculer la concentration, tu utilises la relation : n(titré) = n(titrant) × rapport stœchiométrique. Cette méthode est ultra-précise et très utilisée en laboratoire pour analyser les eaux minérales.

Qualité et potabilité : ce qui rend l'eau buvable
Alors, qu'est-ce qui fait qu'une eau est potable ? C'est plus complexe que tu ne le penses ! L'eau naturelle n'est jamais pure et peut contenir des trucs pas terribles pour ta santé.
Une eau potable ne doit contenir aucune substance nocive : pas de germes pathogènes (bactéries, virus), pas de métaux lourds, pas de pesticides ou d'hydrocarbures. Par contre, elle doit garder les sels minéraux essentiels comme le calcium et le magnésium.
Les critères de potabilité se regroupent en 5 paramètres :
- Physico-chimiques : pH entre 6,5 et 9, sulfates <250 mg/L, chlorures <200 mg/L
- Organoleptiques : couleur, goût, odeur agréables
- Microbiologiques : zéro germe pathogène
- Substances indésirables : nitrates <50 mg/L, fluor <1,5 mg/L
- Substances toxiques : normes ultra-strictes (millionième de gramme)
💡 Bon à savoir : Une eau trop "douce" peut corroder les canalisations !
Le titre hydrotimétrique (TH) mesure la dureté de l'eau et doit être >15°f pour éviter la corrosion des tuyaux.

Exercices pratiques : maîtriser les calculs
Ces exercices te font bosser les relations concentration-conductivité et les dosages par titrage. Super utile pour tes évaluations !
L'exercice 1 compare deux solutions ioniques de même concentration. Tu dois identifier quel conductimètre mesure la conductivité et expliquer pourquoi une solution conduit mieux qu'une autre.
L'exercice 2 travaille sur l'étiquette d'une eau minérale. Tu convertis les concentrations massiques en concentrations molaires en utilisant les masses molaires. N'oublie pas de bien convertir mg en g !
💡 Méthode : Pour passer de mg/L à mol/L, divise par la masse molaire et multiplie par 10⁻³.
L'exercice 5 est un dosage conductimétrique complet des ions chlorure. Tu écris l'équation de réaction, définis l'équivalence, détermines Veq graphiquement, puis calcules la concentration recherchée.
Ces exercices te préparent parfaitement aux situations d'examen en combinant théorie et applications concrètes !

Corrections détaillées : comprendre tes erreurs
Les corrections te montrent la méthode complète pour chaque calcul. C'est là que tu vois si tu maîtrises vraiment !
Pour l'exercice 2, la conversion des hydrogénocarbonates : 219 mg/L = 0,219 g/L. Avec M(HCO₃⁻) = 61 g/mol, tu obtiens n = 3,6×10⁻³ mol dans 1L.
La concentration molaire devient donc C = 3,6×10⁻³ mol/L. Simple quand on connaît la formule n = Cm/M !
💡 Piège classique : Attention aux unités ! Toujours vérifier mg→g et L dans les calculs.
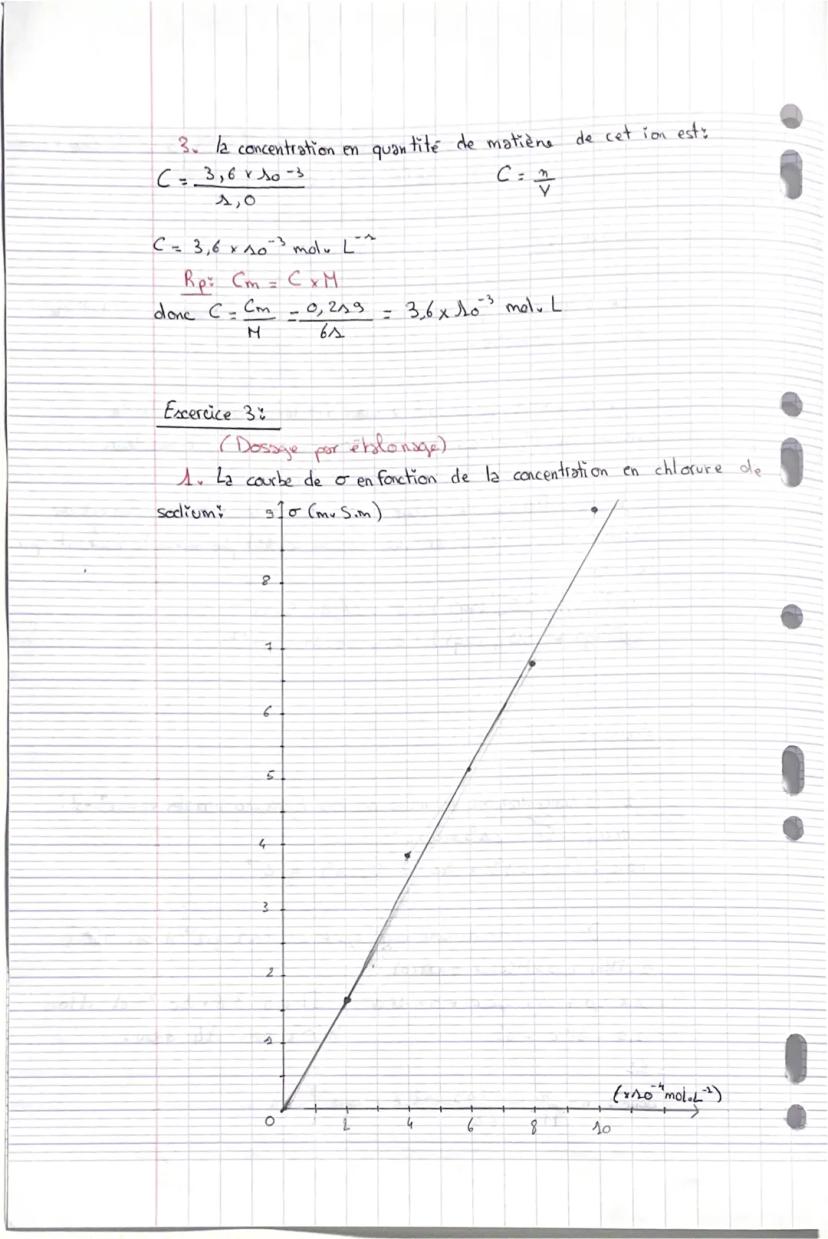
Pour l'exercice 3, la relation de proportionnalité entre conductivité et concentration est linéaire. La droite passe par l'origine, ce qui confirme que σ = k×C (avec k constante).
Ces corrections te donnent les réflexes pour éviter les erreurs types : oubli de conversion d'unités, mauvaise lecture graphique, ou erreur de formule.
Graphiques et calculs avancés
Cette page te montre comment tracer et exploiter correctement une courbe de conductivité. C'est un savoir-faire indispensable !
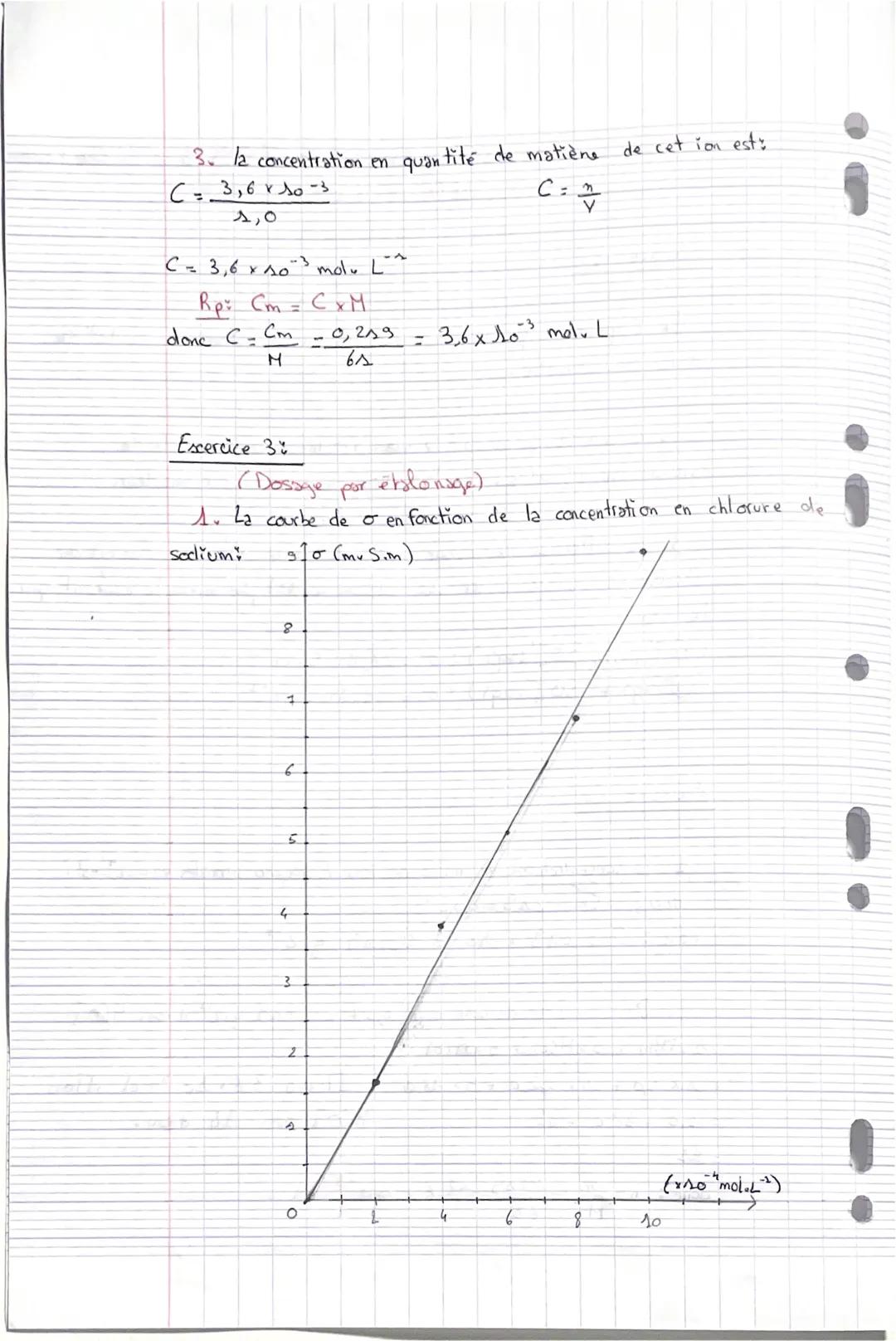
La courbe σ = f(C) pour le chlorure de sodium donne une droite parfaite qui passe par l'origine. Cette proportionnalité directe est caractéristique des solutions ioniques diluées.
Pour trouver la concentration d'eau de mer, tu lis σ = 6,4 mS/m sur ton graphique, ce qui correspond à C = 7,5×10⁻⁴ mol/L en NaCl.
💡 Lecture graphique : Trace bien tes droites et lis précisément les coordonnées des points !
Cette méthode d'étalonnage est super pratique : tu établis une courbe de référence avec des solutions de concentration connue, puis tu y lis directement la concentration d'un échantillon inconnu.
Dosage par titrage : la pratique complète
Ici tu vois un dosage par titrage en action avec tous les détails pratiques. C'est du concret !
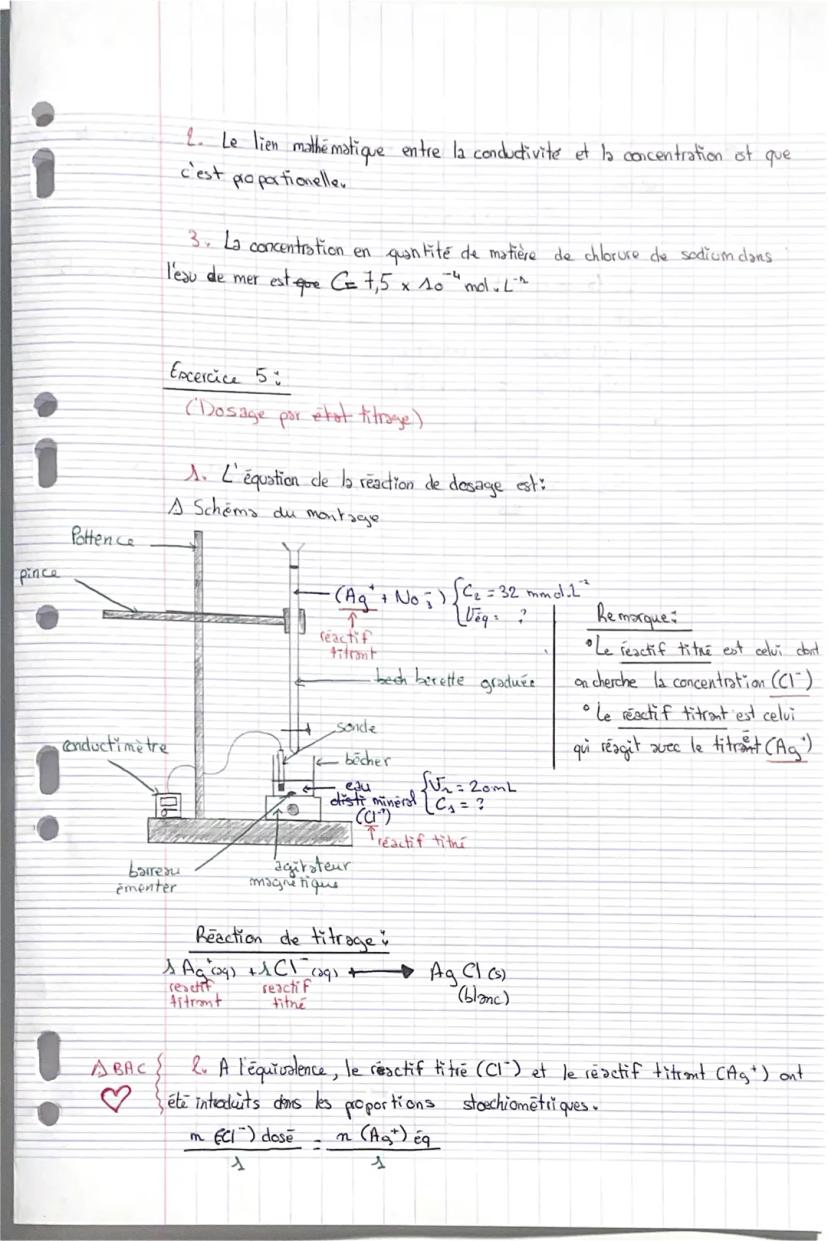
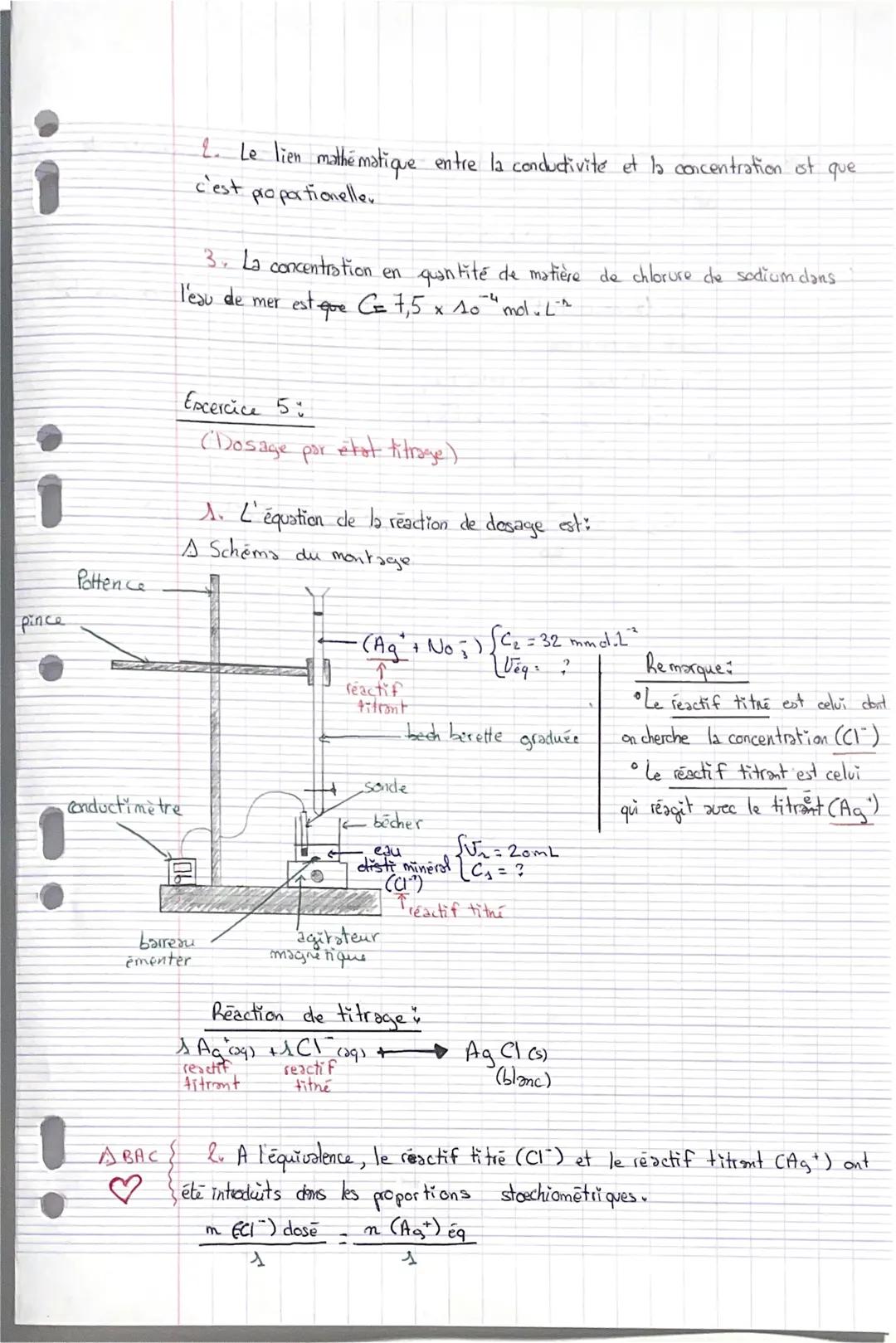
L'équation de réaction est Ag⁺ + Cl⁻ → AgCl(s). Le précipité blanc d'AgCl se forme progressivement. Le réactif titré (Cl⁻) est celui dont on cherche la concentration, le réactif titrant (Ag⁺) a une concentration connue.
Le montage comprend une burette graduée contenant la solution titrante, un bécher avec l'échantillon, un conductimètre avec sa sonde, et un agitateur magnétique.
💡 Définition clé : À l'équivalence, n(Cl⁻)dose = n(Ag⁺)eq selon la stœchiométrie 1:1.
Sur la courbe, Veq correspond à l'intersection des deux segments de droite. Ici Veq = 4,5 mL. Cette valeur est cruciale pour tous tes calculs suivants !

Calculs finaux et résultats
La dernière étape : transformer tes mesures en concentration réelle ! C'est là que tout se concrétise.
Avec Veq = 4,5 mL et les volumes/concentrations de départ, tu appliques la relation d'équivalence : C₁×V₁ = C₂×Veq.
Le calcul donne : C(Cl⁻) = (32×10⁻³ × 4,5×10⁻³)/20×10⁻³ = 7,2×10⁻³ mol/L. Puis tu convertis en concentration massique : Cm = C × M(Cl) = 7,2×10⁻³ × 35,5 = 0,256 g/L.
💡 Vérification : Compare toujours ton résultat avec la valeur annoncée sur l'étiquette !
Cette méthode de dosage conductimétrique te donne une précision excellente pour l'analyse quantitative des ions. C'est une technique de référence dans tous les laboratoires d'analyse d'eau !
Si on te demande...
Qu'est-ce que le compagnon IA de Knowunity ?
Notre compagnon IA est spécialement conçu pour répondre aux besoins des étudiants. Sur la base des millions d'éléments de contenu que nous avons sur la plateforme, nous pouvons fournir des réponses vraiment significatives et pertinentes aux étudiants. Mais il ne s'agit pas seulement de réponses, le compagnon a encore plus pour but de guider les élèves dans leurs défis d'apprentissage quotidiens, avec des plans d'étude personnalisés, des quiz ou des éléments de contenu dans le chat et une personnalisation à 100% basée sur les compétences et les développements de l'étudiant.
Où puis-je télécharger l'appli Knowunity ?
Tu peux télécharger l'application dans Google Play Store et dans l'App Store d'Apple.
L'application est-elle vraiment gratuite ?
Oui, tu as un accès entièrement gratuit à tous les contenus de l'appli, tu peux chatter ou suivre les créateurs à tout moment. De plus, nous proposons Knowunity Premium, qui te permet de réviser sans limites!
Contenus similaires
Contenus les plus populaires : conducteur
6Titrage Conductimétrique
Explorez les principes du titrage conductimétrique, y compris les calculs de conductance, la relation de Kohlrausch, et l'importance de l'équivalence dans les titrages acido-basiques. Ce document est une ressource essentielle pour les étudiants en Terminale spécialité Physique-Chimie, offrant des explications claires et des schémas de montage pour une meilleure compréhension.
Conductance et Conductivité
Explorez les concepts de conductance et de conductivité, y compris la loi d'Ohm et la loi de Kohlraush. Ce résumé aborde les calculs de conductivité, les relations entre intensité, tension et résistance, ainsi que des exemples pratiques. Type de contenu : résumé.
Propriétés des Métaux
Explorez les propriétés des métaux, y compris la conductivité électrique, les transformations chimiques dans les piles électrochimiques, et les caractéristiques distinctives des métaux courants comme le fer, l'aluminium et le cuivre. Ce résumé aborde les concepts clés tels que la conduction électrique, les métaux ferreux et non ferreux, et les alliages, offrant une compréhension approfondie pour les étudiants en physique et chimie.
Ions et pH en Chimie
Explorez les concepts clés des ions et du pH dans ce cours de physique-chimie de 3ème. Apprenez à reconnaître les ions métalliques, comprendre les précautions de sécurité, et maîtriser les notions d'acidité et de basicité. Idéal pour les étudiants souhaitant approfondir leurs connaissances en chimie.
Titrage et Conductimétrie
Explorez les méthodes d'analyse chimique, notamment le titrage acide-base et la conductimétrie. Ce document couvre les concepts clés tels que le point d'équivalence, la concentration molaire, et les calculs chimiques nécessaires pour une analyse précise. Idéal pour les étudiants en chimie cherchant à maîtriser ces techniques essentielles.
Cations et Anions
Explorez la formation et la stabilité des cations et anions, ainsi que leur rôle dans la conduction électrique des solutions. Ce résumé aborde les concepts clés des ions chimiques, leur charge et leur importance dans les solutions. Type: résumé.
Contenus les plus populaires en Physique/Chimie
9Des atomes aux ions
Comprendre comment un atome devient un ion par la perte ou le gain d'électrons tout en conservant son noyau intact.
Révisions Physique-Chimie Bac
Explorez les concepts clés de la physique et de la chimie pour le bac avec ces fiches de révision. Couvrez des sujets tels que les réactions acido-basiques, les transferts thermiques, les lois de Kepler, et bien plus. Idéal pour préparer efficacement votre examen de terminale générale.
Formules Clés Physique-Chimie
Découvrez les formules essentielles de Physique-Chimie pour la terminale, incluant la densité, la loi d'Ohm, la concentration molaire, et bien plus. Idéal pour préparer le bac et maîtriser les concepts fondamentaux. Type: résumé.
Les atomes et les molécules
Physique chimie - les atomes et les molécules
Équations Chimiques Équilibrées
Explorez les principes des transformations chimiques et la conservation de la masse à travers des exemples d'équations chimiques équilibrées. Ce contenu aborde les concepts clés tels que la synthèse chimique, les réactions de combustion, et les méthodes pour équilibrer les équations. Idéal pour les étudiants en chimie cherchant à comprendre les bases des transformations chimiques.
Définition et Formation des Ions
Comprendre comment un atome devient un ion positif ou négatif en perdant ou gagnant des électrons.
Formules Clés Physique-Chimie Bac
Cette fiche de révision présente les formules essentielles de physique et chimie à maîtriser pour réussir le bac. Idéale pour les étudiants préparant leur examen, elle couvre les concepts fondamentaux et les équations cruciales à connaître.
Comprendre les Ions
Explorez la définition des ions, leur classification en cations et anions, ainsi que les méthodes d'identification des ions en chimie. Ce document de méthode est conçu pour les élèves de 3ème et aborde les concepts clés tels que la formation des ions et les tests d'identification. Idéal pour maîtriser les bases de la chimie des ions.
Formulaire Physique STI2D
Ce formulaire complet couvre les principes fondamentaux de la physique pour la terminale STI2D, incluant la mécanique, l'électricité, l'énergie, et les transferts thermiques. Idéal pour réviser les concepts clés tels que la puissance, l'énergie cinétique, et les lois de l'électricité. Type : résumé.
Contenus les plus populaires
9Guerre Totale : 1939-1945
Explorez les événements marquants de la Seconde Guerre mondiale, de l'invasion de la Pologne à la capitulation du Japon. Ce résumé aborde les concepts clés tels que la guerre totale, le génocide des Juifs, la bataille de Stalingrad, et l'impact de la propagande. Idéal pour les étudiants en histoire cherchant à comprendre les enjeux et les conséquences de ce conflit majeur.
Introduction à la Seconde Guerre mondiale
Identifiez les causes du conflit, les alliances et les dates clés du déclenchement de la guerre en Europe et dans le Pacifique.
Conscience en Philosophie
Explorez la notion de conscience en philosophie à travers ses implications sur la justice, la liberté, et la connaissance. Cette fiche de révision aborde les débats philosophiques sur la conscience, le cogito, et les valeurs morales, tout en intégrant des perspectives contemporaines. Idéale pour les étudiants en philosophie cherchant à approfondir leur compréhension des enjeux éthiques et existentiels.
Défaite de 1940 et Régime de Vichy
Comprendre l'armistice de juin 1940, la fin de la IIIe République et la mise en place du nouveau régime autoritaire de Philippe Pétain.
Figures de Style Essentielles
Explorez les figures de style clés pour enrichir vos commentaires composés et oraux du Bac de Français. Ce document présente des définitions claires et des exemples illustratifs pour chaque figure, y compris la métaphore, la comparaison, et la personnification. Idéal pour les étudiants préparant le Bac.
Guerre Froide : Conflits et Idéologies
Explorez les événements clés de la Guerre Froide (1947-1991), y compris le Plan Marshall, la crise de Berlin, la guerre de Corée et la crise de Cuba. Ce résumé met en lumière les tensions entre le communisme et le capitalisme, ainsi que les conséquences de cette période sur le monde moderne. Type : résumé de cours BAC PRO.
Combat pour l'Égalité
Analyse approfondie du 'Discours de la servitude volontaire' d'Étienne de la Boétie, explorant les thèmes de la tyrannie, de la désobéissance civile et des droits du peuple. Ce document est conçu pour aider à la préparation de l'oral du bac de français, en mettant l'accent sur la lutte pour l'égalité et la liberté. Idéal pour les étudiants souhaitant comprendre les enjeux de la servitude volontaire et son impact sur la pensée politique moderne.
Citations par thème, le discours de la servitude volontaire
Citations, Œuvres reliées, par idées sur le Discours de la Servitude Volontaire de Étienne de La Boetie
Amazon : Performance et Conditions de Travail
Explorez l'étude de gestion sur Amazon, mettant en lumière la relation entre performance sociale et commerciale. Ce dossier aborde l'impact des conditions de travail sur la performance de l'entreprise, ainsi que les stratégies de croissance et d'innovation technologique. Idéal pour les étudiants en gestion souhaitant comprendre les enjeux contemporains du e-commerce. Type : Synthèse d'étude de gestion.
Rien ne te convient ? Explore d'autres matières.
Les étudiants nous adorent — il ne manque plus que toi.
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Comprendre la qualité de l'eau
Salut ! On va explorer la qualité de l'eau, un sujet super pratique pour comprendre ce qu'on boit tous les jours. Tu vas découvrir comment l'eau conduit l'électricité, comment on mesure la concentration des ions, et surtout quels critères rendent... Affiche plus

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Solubilité et conductivité : les bases de la chimie de l'eau
Tu sais que l'eau du robinet conduit l'électricité ? C'est grâce aux ions dissous qu'elle contient ! L'eau pure (H₂O) est une molécule polaire : l'oxygène est légèrement négatif, les hydrogènes légèrement positifs.
Cette polarité permet à l'eau de dissoudre facilement les solides ioniques comme le sel de cuisine (NaCl). La solubilité te dit combien de grammes maximum tu peux dissoudre dans 1 L d'eau. Par exemple, le sel a une solubilité de 358,5 g/L à 25°C.
Quand un solide ionique se dissout, il libère ses ions dans l'eau : NaCl(s) → Na⁺(aq) + Cl⁻(aq). Ces ions bougent librement et permettent le passage du courant électrique.
💡 Astuce pratique : Plus une eau contient d'ions, mieux elle conduit l'électricité. C'est pourquoi l'eau distillée (sans ions) ne conduit pas du tout !
La conductivité se mesure avec un conductimètre en siemens par mètre . Elle dépend de la nature des ions, leur concentration, et la température de la solution.

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Dosage par titrage conductimétrique : mesurer précisément les ions
Le titrage conductimétrique est ta technique de référence pour connaître la concentration exacte d'un ion dans l'eau. C'est comme une recette de cuisine chimique !
Le principe est simple : tu verses progressivement une solution titrante (concentration connue) dans ta solution titrée (concentration inconnue). À chaque ajout, tu mesures la conductivité avec ton conductimètre.
La courbe obtenue forme deux segments de droite qui se croisent au point d'équivalence. C'est le moment magique où tous tes ions ont réagi dans les bonnes proportions ! L'abscisse de ce point te donne le volume équivalent Veq.
💡 Formule clé : À l'équivalence, les réactifs respectent la stœchiométrie de l'équation de réaction.
Pour calculer la concentration, tu utilises la relation : n(titré) = n(titrant) × rapport stœchiométrique. Cette méthode est ultra-précise et très utilisée en laboratoire pour analyser les eaux minérales.

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Qualité et potabilité : ce qui rend l'eau buvable
Alors, qu'est-ce qui fait qu'une eau est potable ? C'est plus complexe que tu ne le penses ! L'eau naturelle n'est jamais pure et peut contenir des trucs pas terribles pour ta santé.
Une eau potable ne doit contenir aucune substance nocive : pas de germes pathogènes (bactéries, virus), pas de métaux lourds, pas de pesticides ou d'hydrocarbures. Par contre, elle doit garder les sels minéraux essentiels comme le calcium et le magnésium.
Les critères de potabilité se regroupent en 5 paramètres :
- Physico-chimiques : pH entre 6,5 et 9, sulfates <250 mg/L, chlorures <200 mg/L
- Organoleptiques : couleur, goût, odeur agréables
- Microbiologiques : zéro germe pathogène
- Substances indésirables : nitrates <50 mg/L, fluor <1,5 mg/L
- Substances toxiques : normes ultra-strictes (millionième de gramme)
💡 Bon à savoir : Une eau trop "douce" peut corroder les canalisations !
Le titre hydrotimétrique (TH) mesure la dureté de l'eau et doit être >15°f pour éviter la corrosion des tuyaux.

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Exercices pratiques : maîtriser les calculs
Ces exercices te font bosser les relations concentration-conductivité et les dosages par titrage. Super utile pour tes évaluations !
L'exercice 1 compare deux solutions ioniques de même concentration. Tu dois identifier quel conductimètre mesure la conductivité et expliquer pourquoi une solution conduit mieux qu'une autre.
L'exercice 2 travaille sur l'étiquette d'une eau minérale. Tu convertis les concentrations massiques en concentrations molaires en utilisant les masses molaires. N'oublie pas de bien convertir mg en g !
💡 Méthode : Pour passer de mg/L à mol/L, divise par la masse molaire et multiplie par 10⁻³.
L'exercice 5 est un dosage conductimétrique complet des ions chlorure. Tu écris l'équation de réaction, définis l'équivalence, détermines Veq graphiquement, puis calcules la concentration recherchée.
Ces exercices te préparent parfaitement aux situations d'examen en combinant théorie et applications concrètes !

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Corrections détaillées : comprendre tes erreurs
Les corrections te montrent la méthode complète pour chaque calcul. C'est là que tu vois si tu maîtrises vraiment !
Pour l'exercice 2, la conversion des hydrogénocarbonates : 219 mg/L = 0,219 g/L. Avec M(HCO₃⁻) = 61 g/mol, tu obtiens n = 3,6×10⁻³ mol dans 1L.
La concentration molaire devient donc C = 3,6×10⁻³ mol/L. Simple quand on connaît la formule n = Cm/M !
💡 Piège classique : Attention aux unités ! Toujours vérifier mg→g et L dans les calculs.
Pour l'exercice 3, la relation de proportionnalité entre conductivité et concentration est linéaire. La droite passe par l'origine, ce qui confirme que σ = k×C (avec k constante).
Ces corrections te donnent les réflexes pour éviter les erreurs types : oubli de conversion d'unités, mauvaise lecture graphique, ou erreur de formule.

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Graphiques et calculs avancés
Cette page te montre comment tracer et exploiter correctement une courbe de conductivité. C'est un savoir-faire indispensable !
La courbe σ = f(C) pour le chlorure de sodium donne une droite parfaite qui passe par l'origine. Cette proportionnalité directe est caractéristique des solutions ioniques diluées.
Pour trouver la concentration d'eau de mer, tu lis σ = 6,4 mS/m sur ton graphique, ce qui correspond à C = 7,5×10⁻⁴ mol/L en NaCl.
💡 Lecture graphique : Trace bien tes droites et lis précisément les coordonnées des points !
Cette méthode d'étalonnage est super pratique : tu établis une courbe de référence avec des solutions de concentration connue, puis tu y lis directement la concentration d'un échantillon inconnu.

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Dosage par titrage : la pratique complète
Ici tu vois un dosage par titrage en action avec tous les détails pratiques. C'est du concret !
L'équation de réaction est Ag⁺ + Cl⁻ → AgCl(s). Le précipité blanc d'AgCl se forme progressivement. Le réactif titré (Cl⁻) est celui dont on cherche la concentration, le réactif titrant (Ag⁺) a une concentration connue.
Le montage comprend une burette graduée contenant la solution titrante, un bécher avec l'échantillon, un conductimètre avec sa sonde, et un agitateur magnétique.
💡 Définition clé : À l'équivalence, n(Cl⁻)dose = n(Ag⁺)eq selon la stœchiométrie 1:1.
Sur la courbe, Veq correspond à l'intersection des deux segments de droite. Ici Veq = 4,5 mL. Cette valeur est cruciale pour tous tes calculs suivants !

Inscris-toi pour voir le contenu. C'est gratuit!
- Accès à tous les documents
- Améliore tes notes
- Rejoins des millions d'étudiants
Calculs finaux et résultats
La dernière étape : transformer tes mesures en concentration réelle ! C'est là que tout se concrétise.
Avec Veq = 4,5 mL et les volumes/concentrations de départ, tu appliques la relation d'équivalence : C₁×V₁ = C₂×Veq.
Le calcul donne : C(Cl⁻) = (32×10⁻³ × 4,5×10⁻³)/20×10⁻³ = 7,2×10⁻³ mol/L. Puis tu convertis en concentration massique : Cm = C × M(Cl) = 7,2×10⁻³ × 35,5 = 0,256 g/L.
💡 Vérification : Compare toujours ton résultat avec la valeur annoncée sur l'étiquette !
Cette méthode de dosage conductimétrique te donne une précision excellente pour l'analyse quantitative des ions. C'est une technique de référence dans tous les laboratoires d'analyse d'eau !
Si on te demande...
Qu'est-ce que le compagnon IA de Knowunity ?
Notre compagnon IA est spécialement conçu pour répondre aux besoins des étudiants. Sur la base des millions d'éléments de contenu que nous avons sur la plateforme, nous pouvons fournir des réponses vraiment significatives et pertinentes aux étudiants. Mais il ne s'agit pas seulement de réponses, le compagnon a encore plus pour but de guider les élèves dans leurs défis d'apprentissage quotidiens, avec des plans d'étude personnalisés, des quiz ou des éléments de contenu dans le chat et une personnalisation à 100% basée sur les compétences et les développements de l'étudiant.
Où puis-je télécharger l'appli Knowunity ?
Tu peux télécharger l'application dans Google Play Store et dans l'App Store d'Apple.
L'application est-elle vraiment gratuite ?
Oui, tu as un accès entièrement gratuit à tous les contenus de l'appli, tu peux chatter ou suivre les créateurs à tout moment. De plus, nous proposons Knowunity Premium, qui te permet de réviser sans limites!
Contenus similaires
Contenus les plus populaires : conducteur
6Titrage Conductimétrique
Explorez les principes du titrage conductimétrique, y compris les calculs de conductance, la relation de Kohlrausch, et l'importance de l'équivalence dans les titrages acido-basiques. Ce document est une ressource essentielle pour les étudiants en Terminale spécialité Physique-Chimie, offrant des explications claires et des schémas de montage pour une meilleure compréhension.
Conductance et Conductivité
Explorez les concepts de conductance et de conductivité, y compris la loi d'Ohm et la loi de Kohlraush. Ce résumé aborde les calculs de conductivité, les relations entre intensité, tension et résistance, ainsi que des exemples pratiques. Type de contenu : résumé.
Propriétés des Métaux
Explorez les propriétés des métaux, y compris la conductivité électrique, les transformations chimiques dans les piles électrochimiques, et les caractéristiques distinctives des métaux courants comme le fer, l'aluminium et le cuivre. Ce résumé aborde les concepts clés tels que la conduction électrique, les métaux ferreux et non ferreux, et les alliages, offrant une compréhension approfondie pour les étudiants en physique et chimie.
Ions et pH en Chimie
Explorez les concepts clés des ions et du pH dans ce cours de physique-chimie de 3ème. Apprenez à reconnaître les ions métalliques, comprendre les précautions de sécurité, et maîtriser les notions d'acidité et de basicité. Idéal pour les étudiants souhaitant approfondir leurs connaissances en chimie.
Titrage et Conductimétrie
Explorez les méthodes d'analyse chimique, notamment le titrage acide-base et la conductimétrie. Ce document couvre les concepts clés tels que le point d'équivalence, la concentration molaire, et les calculs chimiques nécessaires pour une analyse précise. Idéal pour les étudiants en chimie cherchant à maîtriser ces techniques essentielles.
Cations et Anions
Explorez la formation et la stabilité des cations et anions, ainsi que leur rôle dans la conduction électrique des solutions. Ce résumé aborde les concepts clés des ions chimiques, leur charge et leur importance dans les solutions. Type: résumé.
Contenus les plus populaires en Physique/Chimie
9Des atomes aux ions
Comprendre comment un atome devient un ion par la perte ou le gain d'électrons tout en conservant son noyau intact.
Révisions Physique-Chimie Bac
Explorez les concepts clés de la physique et de la chimie pour le bac avec ces fiches de révision. Couvrez des sujets tels que les réactions acido-basiques, les transferts thermiques, les lois de Kepler, et bien plus. Idéal pour préparer efficacement votre examen de terminale générale.
Formules Clés Physique-Chimie
Découvrez les formules essentielles de Physique-Chimie pour la terminale, incluant la densité, la loi d'Ohm, la concentration molaire, et bien plus. Idéal pour préparer le bac et maîtriser les concepts fondamentaux. Type: résumé.
Les atomes et les molécules
Physique chimie - les atomes et les molécules
Équations Chimiques Équilibrées
Explorez les principes des transformations chimiques et la conservation de la masse à travers des exemples d'équations chimiques équilibrées. Ce contenu aborde les concepts clés tels que la synthèse chimique, les réactions de combustion, et les méthodes pour équilibrer les équations. Idéal pour les étudiants en chimie cherchant à comprendre les bases des transformations chimiques.
Définition et Formation des Ions
Comprendre comment un atome devient un ion positif ou négatif en perdant ou gagnant des électrons.
Formules Clés Physique-Chimie Bac
Cette fiche de révision présente les formules essentielles de physique et chimie à maîtriser pour réussir le bac. Idéale pour les étudiants préparant leur examen, elle couvre les concepts fondamentaux et les équations cruciales à connaître.
Comprendre les Ions
Explorez la définition des ions, leur classification en cations et anions, ainsi que les méthodes d'identification des ions en chimie. Ce document de méthode est conçu pour les élèves de 3ème et aborde les concepts clés tels que la formation des ions et les tests d'identification. Idéal pour maîtriser les bases de la chimie des ions.
Formulaire Physique STI2D
Ce formulaire complet couvre les principes fondamentaux de la physique pour la terminale STI2D, incluant la mécanique, l'électricité, l'énergie, et les transferts thermiques. Idéal pour réviser les concepts clés tels que la puissance, l'énergie cinétique, et les lois de l'électricité. Type : résumé.
Contenus les plus populaires
9Guerre Totale : 1939-1945
Explorez les événements marquants de la Seconde Guerre mondiale, de l'invasion de la Pologne à la capitulation du Japon. Ce résumé aborde les concepts clés tels que la guerre totale, le génocide des Juifs, la bataille de Stalingrad, et l'impact de la propagande. Idéal pour les étudiants en histoire cherchant à comprendre les enjeux et les conséquences de ce conflit majeur.
Introduction à la Seconde Guerre mondiale
Identifiez les causes du conflit, les alliances et les dates clés du déclenchement de la guerre en Europe et dans le Pacifique.
Conscience en Philosophie
Explorez la notion de conscience en philosophie à travers ses implications sur la justice, la liberté, et la connaissance. Cette fiche de révision aborde les débats philosophiques sur la conscience, le cogito, et les valeurs morales, tout en intégrant des perspectives contemporaines. Idéale pour les étudiants en philosophie cherchant à approfondir leur compréhension des enjeux éthiques et existentiels.
Défaite de 1940 et Régime de Vichy
Comprendre l'armistice de juin 1940, la fin de la IIIe République et la mise en place du nouveau régime autoritaire de Philippe Pétain.
Figures de Style Essentielles
Explorez les figures de style clés pour enrichir vos commentaires composés et oraux du Bac de Français. Ce document présente des définitions claires et des exemples illustratifs pour chaque figure, y compris la métaphore, la comparaison, et la personnification. Idéal pour les étudiants préparant le Bac.
Guerre Froide : Conflits et Idéologies
Explorez les événements clés de la Guerre Froide (1947-1991), y compris le Plan Marshall, la crise de Berlin, la guerre de Corée et la crise de Cuba. Ce résumé met en lumière les tensions entre le communisme et le capitalisme, ainsi que les conséquences de cette période sur le monde moderne. Type : résumé de cours BAC PRO.
Combat pour l'Égalité
Analyse approfondie du 'Discours de la servitude volontaire' d'Étienne de la Boétie, explorant les thèmes de la tyrannie, de la désobéissance civile et des droits du peuple. Ce document est conçu pour aider à la préparation de l'oral du bac de français, en mettant l'accent sur la lutte pour l'égalité et la liberté. Idéal pour les étudiants souhaitant comprendre les enjeux de la servitude volontaire et son impact sur la pensée politique moderne.
Citations par thème, le discours de la servitude volontaire
Citations, Œuvres reliées, par idées sur le Discours de la Servitude Volontaire de Étienne de La Boetie
Amazon : Performance et Conditions de Travail
Explorez l'étude de gestion sur Amazon, mettant en lumière la relation entre performance sociale et commerciale. Ce dossier aborde l'impact des conditions de travail sur la performance de l'entreprise, ainsi que les stratégies de croissance et d'innovation technologique. Idéal pour les étudiants en gestion souhaitant comprendre les enjeux contemporains du e-commerce. Type : Synthèse d'étude de gestion.
Rien ne te convient ? Explore d'autres matières.
Les étudiants nous adorent — il ne manque plus que toi.
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.