Tu vas découvrir les transformations chimiques et leur caractère total... Affiche plus
Inscris-toi pour voir le contenuC'est gratuit!
Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Knowunity AI
Matières
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Affiche tous les sujets
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Affiche tous les sujets
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Affiche tous les sujets
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Affiche tous les sujets
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Affiche tous les sujets
221
•
Mis à jour May 16, 2026
•
SuRaYa
@suraya_a
Tu vas découvrir les transformations chimiques et leur caractère total... Affiche plus







Imagine que tu mélanges des réactifs : selon les conditions, la réaction peut aller jusqu'au bout ou s'arrêter avant. C'est exactement ce qui distingue les transformations totales des transformations équilibrées.
Dans une transformation totale, au moins un réactif disparaît complètement. On l'appelle le réactif limitant car c'est lui qui détermine quand la réaction s'arrête. Les autres réactifs sont en excès. Tu notes cette réaction avec une simple flèche : réactifs → produits, et l'avancement final égale l'avancement maximal $x_f = x_{max}$.
Pour une transformation équilibrée, aucun réactif n'est totalement consommé. La réaction semble s'arrêter avant la fin, créant un équilibre entre réactifs et produits. Tu utilises une double flèche ⇌ pour les transformations chimiques ou le signe = pour les dissociations. Ici, .
À retenir : L'eau est généralement toujours en excès dans tes calculs !

Le taux d'avancement final te permet de quantifier à quel point une réaction a progressé. C'est un outil super pratique pour comparer différentes réactions !
La formule est simple : (ou × 100 pour un pourcentage). Si T = 1 (ou 100%), ta réaction est totale. Si T < 1 (ou < 100%), ta réaction est équilibrée.
Plus le taux d'avancement est élevé, plus tu te rapproches d'une réaction totale. C'est comme un indicateur de "performance" de ta réaction. Un T de 0,8 (80%) signifie que 80% de ce qui pouvait réagir a effectivement réagi.
Cette notion te sera très utile pour tes exercices car elle permet de caractériser rapidement le type de transformation que tu étudies.

Le quotient de réaction Qr est ton outil de prédiction : il te dit dans quel sens va évoluer ta réaction ! Pour une réaction aA + bB ⇌ cC + dD, tu calcules : .
Attention aux règles spéciales : si une espèce est solide ou si c'est le solvant, tu remplaces sa concentration par 1. Les crochets [ ] représentent toujours des concentrations en mol/L.
La constante d'équilibre K(T) correspond au quotient de réaction à l'état final d'équilibre. Elle dépend uniquement de la température, d'où le (T).
Le critère d'évolution est génial pour prévoir l'évolution spontanée : si Qr < K(T), la réaction va dans le sens direct (formation des produits). Si Qr > K(T), elle va dans le sens inverse. Si Qr = K(T), c'est l'équilibre !
Astuce : Retiens que Qr compare l'état actuel à l'état d'équilibre final !

Les réactions d'oxydoréduction sont partout autour de toi : dans les piles, la respiration, la rouille... Elles impliquent un transfert d'électrons entre espèces chimiques.
Un oxydant gagne des électrons (il "oxyde" l'autre espèce), tandis qu'un réducteur perd des électrons. Dans une demi-équation, tu écris : oxydant + ne⁻ = réducteur ou réducteur = oxydant + ne⁻.
Pour équilibrer, souviens-toi des règles : ajoute H₂O si tu as des atomes O en plus, ajoute H⁺ si tu as des atomes H en plus. L'oxydant se place toujours à gauche du couple, le réducteur à droite.
Les espèces amphotères comme Fe²⁺ peuvent jouer les deux rôles selon le couple considéré. Dans l'équation-bilan finale, assure-toi que le nombre d'électrons perdus égale celui des électrons gagnés !
Exemple concret : 2Au³⁺ + 3Cu → 2Au + 3Cu²⁺ (l'or oxyde le cuivre)

Un couple d'oxydoréduction relie deux espèces par le transfert d'électrons : Oxydant + ne⁻ = Réducteur. L'oxydant capte des électrons, le réducteur en cède.
Pour équilibrer une demi-équation comme Cr₂O₇²⁻/Cr³⁺, suis la méthode en 5 étapes : équilibre d'abord les éléments autres que H et O, puis l'oxygène avec H₂O, l'hydrogène avec H⁺, les charges avec e⁻, et enfin remplace H⁺ par H₃O⁺.
Les espèces amphotères comme Fe²⁺ peuvent être oxydant dans un couple et réducteur dans un autre . C'est normal et très fréquent !
Maîtrise bien les couples usuels : Cu²⁺/Cu, Br₂/Br⁻, H⁺/H₂... Ils reviennent constamment dans tes exercices.
Conseil méthodique : Toujours vérifier l'équilibrage final en comptant atomes et charges !

Une réaction d'oxydoréduction met en jeu l'oxydant d'un couple et le réducteur d'un autre couple. Le principe fondamental : le nombre d'électrons cédés = nombre d'électrons captés.
Pour écrire l'équation-bilan, écris les deux demi-équations puis ajuste les coefficients pour égaliser les électrons. Exemple : 2Fe²⁺ + I₂ → 2Fe³⁺ + 2I⁻.
Apprends les couples usuels car ils sont incontournables : I₂/I⁻, H₂O₂/H₂O, MnO₄⁻/Mn²⁺... Chaque couple a sa demi-équation spécifique avec le bon nombre d'électrons et les bonnes espèces pour équilibrer.
L'eau oxygénée H₂O₂ est particulière : elle peut être oxydant ou réducteur . C'est un exemple parfait d'espèce amphotère !
Piège à éviter : N'oublie jamais d'équilibrer le nombre d'électrons entre les deux demi-équations !
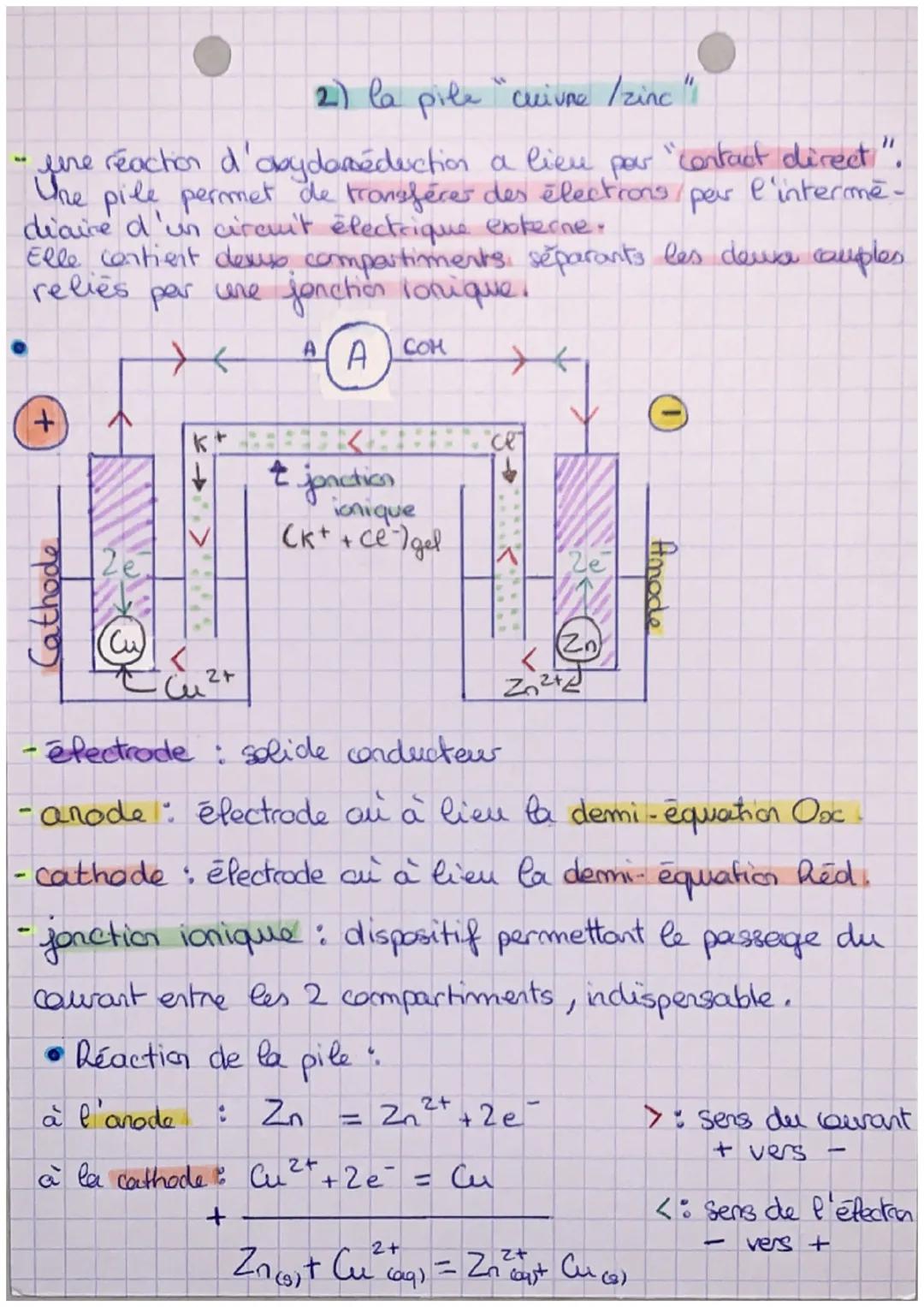
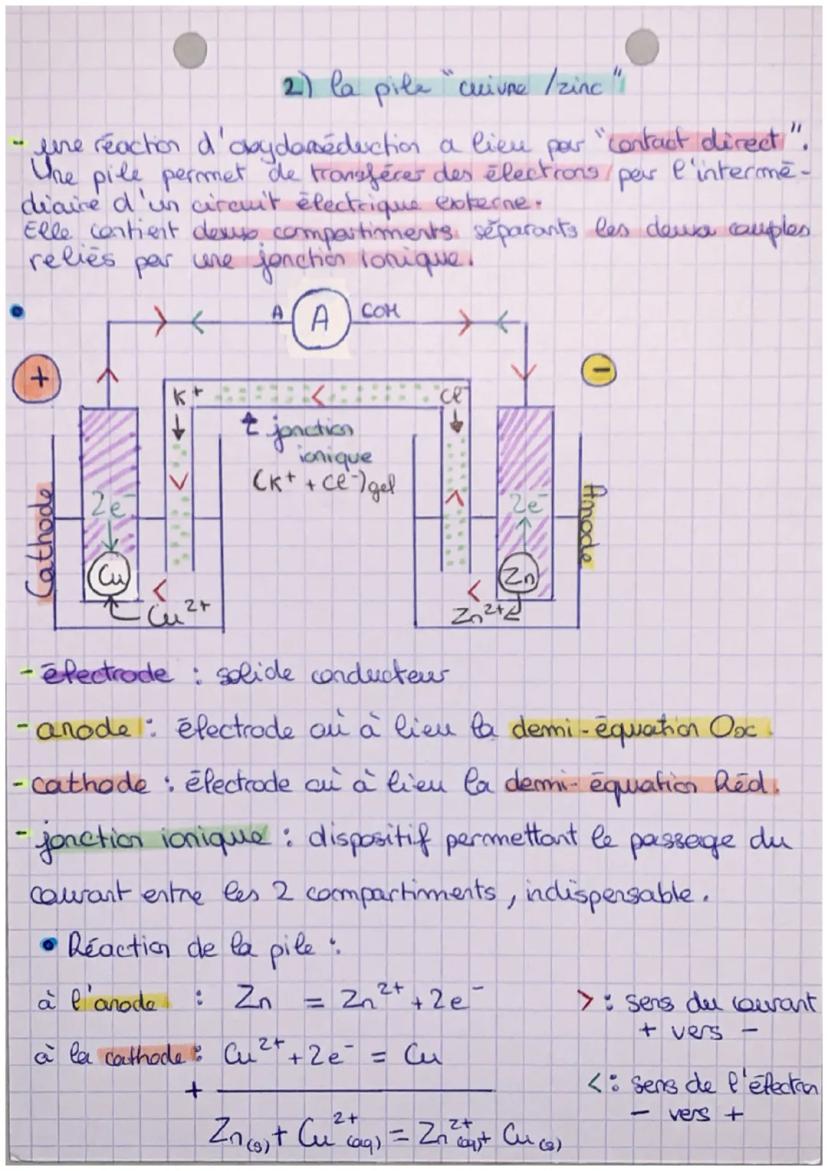
Une pile est un dispositif génial qui exploite une réaction d'oxydoréduction pour produire de l'électricité ! Contrairement au contact direct entre réactifs, elle sépare les deux couples dans des compartiments distincts.
Dans une pile cuivre/zinc, le zinc s'oxyde à l'anode (électrode négative) : Zn → Zn²⁺ + 2e⁻. Le cuivre se réduit à la cathode (électrode positive) : Cu²⁺ + 2e⁻ → Cu. Les électrons circulent de l'anode vers la cathode par le circuit externe.
La jonction ionique (pont salin) est indispensable ! Elle permet aux ions de circuler entre les compartiments pour maintenir l'électroneutralité. Sans elle, la pile ne fonctionne pas.
Retiens le sens : les électrons vont du - vers le +, mais le courant électrique conventionnel va du + vers le -. La réaction globale : Zn + Cu²⁺ → Zn²⁺ + Cu.
Mnémotechnique : "ANOde = OXydation" et "CATHode = REDuction" !
Notre compagnon IA est spécialement conçu pour répondre aux besoins des étudiants. Sur la base des millions d'éléments de contenu que nous avons sur la plateforme, nous pouvons fournir des réponses vraiment significatives et pertinentes aux étudiants. Mais il ne s'agit pas seulement de réponses, le compagnon a encore plus pour but de guider les élèves dans leurs défis d'apprentissage quotidiens, avec des plans d'étude personnalisés, des quiz ou des éléments de contenu dans le chat et une personnalisation à 100% basée sur les compétences et les développements de l'étudiant.
Tu peux télécharger l'application dans Google Play Store et dans l'App Store d'Apple.
Oui, tu as un accès entièrement gratuit à tous les contenus de l'appli, tu peux chatter ou suivre les créateurs à tout moment. De plus, nous proposons Knowunity Premium, qui te permet de réviser sans limites!
App Store
Google Play
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS
SuRaYa
@suraya_a
Tu vas découvrir les transformations chimiques et leur caractère total ou équilibré, ainsi que les réactions d'oxydoréduction. Ces concepts sont essentiels pour comprendre comment les réactions évoluent et prévoir leur comportement.

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Imagine que tu mélanges des réactifs : selon les conditions, la réaction peut aller jusqu'au bout ou s'arrêter avant. C'est exactement ce qui distingue les transformations totales des transformations équilibrées.
Dans une transformation totale, au moins un réactif disparaît complètement. On l'appelle le réactif limitant car c'est lui qui détermine quand la réaction s'arrête. Les autres réactifs sont en excès. Tu notes cette réaction avec une simple flèche : réactifs → produits, et l'avancement final égale l'avancement maximal $x_f = x_{max}$.
Pour une transformation équilibrée, aucun réactif n'est totalement consommé. La réaction semble s'arrêter avant la fin, créant un équilibre entre réactifs et produits. Tu utilises une double flèche ⇌ pour les transformations chimiques ou le signe = pour les dissociations. Ici, .
À retenir : L'eau est généralement toujours en excès dans tes calculs !

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Le taux d'avancement final te permet de quantifier à quel point une réaction a progressé. C'est un outil super pratique pour comparer différentes réactions !
La formule est simple : (ou × 100 pour un pourcentage). Si T = 1 (ou 100%), ta réaction est totale. Si T < 1 (ou < 100%), ta réaction est équilibrée.
Plus le taux d'avancement est élevé, plus tu te rapproches d'une réaction totale. C'est comme un indicateur de "performance" de ta réaction. Un T de 0,8 (80%) signifie que 80% de ce qui pouvait réagir a effectivement réagi.
Cette notion te sera très utile pour tes exercices car elle permet de caractériser rapidement le type de transformation que tu étudies.

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Le quotient de réaction Qr est ton outil de prédiction : il te dit dans quel sens va évoluer ta réaction ! Pour une réaction aA + bB ⇌ cC + dD, tu calcules : .
Attention aux règles spéciales : si une espèce est solide ou si c'est le solvant, tu remplaces sa concentration par 1. Les crochets [ ] représentent toujours des concentrations en mol/L.
La constante d'équilibre K(T) correspond au quotient de réaction à l'état final d'équilibre. Elle dépend uniquement de la température, d'où le (T).
Le critère d'évolution est génial pour prévoir l'évolution spontanée : si Qr < K(T), la réaction va dans le sens direct (formation des produits). Si Qr > K(T), elle va dans le sens inverse. Si Qr = K(T), c'est l'équilibre !
Astuce : Retiens que Qr compare l'état actuel à l'état d'équilibre final !

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Les réactions d'oxydoréduction sont partout autour de toi : dans les piles, la respiration, la rouille... Elles impliquent un transfert d'électrons entre espèces chimiques.
Un oxydant gagne des électrons (il "oxyde" l'autre espèce), tandis qu'un réducteur perd des électrons. Dans une demi-équation, tu écris : oxydant + ne⁻ = réducteur ou réducteur = oxydant + ne⁻.
Pour équilibrer, souviens-toi des règles : ajoute H₂O si tu as des atomes O en plus, ajoute H⁺ si tu as des atomes H en plus. L'oxydant se place toujours à gauche du couple, le réducteur à droite.
Les espèces amphotères comme Fe²⁺ peuvent jouer les deux rôles selon le couple considéré. Dans l'équation-bilan finale, assure-toi que le nombre d'électrons perdus égale celui des électrons gagnés !
Exemple concret : 2Au³⁺ + 3Cu → 2Au + 3Cu²⁺ (l'or oxyde le cuivre)

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Un couple d'oxydoréduction relie deux espèces par le transfert d'électrons : Oxydant + ne⁻ = Réducteur. L'oxydant capte des électrons, le réducteur en cède.
Pour équilibrer une demi-équation comme Cr₂O₇²⁻/Cr³⁺, suis la méthode en 5 étapes : équilibre d'abord les éléments autres que H et O, puis l'oxygène avec H₂O, l'hydrogène avec H⁺, les charges avec e⁻, et enfin remplace H⁺ par H₃O⁺.
Les espèces amphotères comme Fe²⁺ peuvent être oxydant dans un couple et réducteur dans un autre . C'est normal et très fréquent !
Maîtrise bien les couples usuels : Cu²⁺/Cu, Br₂/Br⁻, H⁺/H₂... Ils reviennent constamment dans tes exercices.
Conseil méthodique : Toujours vérifier l'équilibrage final en comptant atomes et charges !

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Une réaction d'oxydoréduction met en jeu l'oxydant d'un couple et le réducteur d'un autre couple. Le principe fondamental : le nombre d'électrons cédés = nombre d'électrons captés.
Pour écrire l'équation-bilan, écris les deux demi-équations puis ajuste les coefficients pour égaliser les électrons. Exemple : 2Fe²⁺ + I₂ → 2Fe³⁺ + 2I⁻.
Apprends les couples usuels car ils sont incontournables : I₂/I⁻, H₂O₂/H₂O, MnO₄⁻/Mn²⁺... Chaque couple a sa demi-équation spécifique avec le bon nombre d'électrons et les bonnes espèces pour équilibrer.
L'eau oxygénée H₂O₂ est particulière : elle peut être oxydant ou réducteur . C'est un exemple parfait d'espèce amphotère !
Piège à éviter : N'oublie jamais d'équilibrer le nombre d'électrons entre les deux demi-équations !

Accès à tous les documents
Améliore tes notes
Rejoins des millions d'étudiants
Une pile est un dispositif génial qui exploite une réaction d'oxydoréduction pour produire de l'électricité ! Contrairement au contact direct entre réactifs, elle sépare les deux couples dans des compartiments distincts.
Dans une pile cuivre/zinc, le zinc s'oxyde à l'anode (électrode négative) : Zn → Zn²⁺ + 2e⁻. Le cuivre se réduit à la cathode (électrode positive) : Cu²⁺ + 2e⁻ → Cu. Les électrons circulent de l'anode vers la cathode par le circuit externe.
La jonction ionique (pont salin) est indispensable ! Elle permet aux ions de circuler entre les compartiments pour maintenir l'électroneutralité. Sans elle, la pile ne fonctionne pas.
Retiens le sens : les électrons vont du - vers le +, mais le courant électrique conventionnel va du + vers le -. La réaction globale : Zn + Cu²⁺ → Zn²⁺ + Cu.
Mnémotechnique : "ANOde = OXydation" et "CATHode = REDuction" !
Notre compagnon IA est spécialement conçu pour répondre aux besoins des étudiants. Sur la base des millions d'éléments de contenu que nous avons sur la plateforme, nous pouvons fournir des réponses vraiment significatives et pertinentes aux étudiants. Mais il ne s'agit pas seulement de réponses, le compagnon a encore plus pour but de guider les élèves dans leurs défis d'apprentissage quotidiens, avec des plans d'étude personnalisés, des quiz ou des éléments de contenu dans le chat et une personnalisation à 100% basée sur les compétences et les développements de l'étudiant.
Tu peux télécharger l'application dans Google Play Store et dans l'App Store d'Apple.
Oui, tu as un accès entièrement gratuit à tous les contenus de l'appli, tu peux chatter ou suivre les créateurs à tout moment. De plus, nous proposons Knowunity Premium, qui te permet de réviser sans limites!
8
Outils Intelligents NOUVEAU
Transforme cette fiche en : ✓ 50+ Questions d'Entraînement ✓ Cartes Mémoire Interactives ✓ Examen blanc complet ✓ Plans de Dissertation
Explorez les concepts clés des acides et des bases, y compris les réactions acido-basiques, le potentiel hydrogène (pH), et les constantes d'acidité (Ka et pKa). Ce résumé aborde la distinction entre acides forts et faibles, ainsi que les bases, et présente des diagrammes de prédominance pour mieux comprendre les espèces chimiques en solution. Idéal pour les étudiants en chimie.
Explorez les concepts clés de l'analyse chimique, y compris la masse volumique, les dosages par titrage direct, et le point d'équivalence. Ce document présente des méthodes de laboratoire essentielles pour comprendre les réactions chimiques et les calculs associés. Type: résumé.
Explorez les propriétés et mécanismes de la réaction d'estérification, y compris les conditions optimales, les rendements expérimentaux et théoriques, ainsi que l'importance de l'hydrolyse. Ce document présente une synthèse chimique détaillée, idéale pour les étudiants en physique et chimie. Type: Synthèse chimique.
Explorez les forces des acides et des bases, y compris les concepts de pKa, les réactions acide-base, et les solutions tampons. Ce document aborde également les diagrammes de prédominance, les indicateurs colorés, et les acides alpha-aminés, offrant une compréhension approfondie des interactions chimiques en solution. Type: résumé.
Explorez les concepts fondamentaux des réactions acido-basiques, y compris les couples acide-base, les demi-équations et les exemples pratiques comme l'interaction entre l'aspirine et l'eau. Ce résumé est essentiel pour comprendre la dynamique des transferts de protons et les espèces amphotères, idéal pour les étudiants en chimie.
Explorez les concepts fondamentaux des acides et des bases, y compris la constante d'acidité (Ka), le pKa, et l'équation de Henderson-Hasselbalch. Ce résumé aborde les solutions tampons, les réactions acido-basiques, et la relation entre pH et concentration. Idéal pour les étudiants en chimie cherchant à comprendre la force des acides et des bases.
App Store
Google Play
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS
L'application est très facile d'utilisation et bien conçue. Jusqu'à présent, j'ai trouvé tout ce que je cherchais et j'ai pu apprendre beaucoup de choses grâce aux présentations ! Je vais certainement utiliser l'application pour un travail en classe ! Et comme source d'inspiration personnelle, elle est bien sûr aussi très utile.
Stefan S
utilisateur iOS
Cette application est vraiment super. Il y a tellement de fiches de révision et d'aide, [...]. Par exemple, la matière qui me pose problème est le français et l'appli a un choix d'aide très large. Grâce à cette application, je me suis améliorée en français. Je la recommanderais à tout le monde.
Samantha Klich
utilisatrice Android
Waouh, je suis vraiment abasourdi. J'ai essayé l'application parce que je l'avais déjà vue plusieurs fois dans la publicité et j'ai été absolument choquée. Cette appli est L'AIDE dont on rêve pour l'école et surtout, elle propose tellement de choses, comme des rédactions et des fiches qui m'ont personnellement TRÈS bien aidé.
Anna
utilisatrice iOS
Meilleur application je voulais m'entraîner pour mes maths puis j'ai tout compris d'un coup c'est mon nouveau prof maintenant 🤣🤣
Thomas R
utilisateur d' Android
super application pour réviser je révise tout les soirs
Esteban M
utilisateur d'Android
Permet de vraiment comprendre les cours sous forme de fiches de révisions déjà faites ! Incroyable, je recommande vraiment
Leny
utilisateur d'Android
L'application est tout simplement géniale ! Il me suffit de taper mon sujet dans la barre de recherche et je le vérifie très rapidement. Je ne dois plus regarder 10 vidéos YouTube pour comprendre quelque chose et j'économise ainsi mon temps. Je te le recommande !
Sudenaz Ocak
utilisateur Android
Cette application m'a vraiment fait m'améliorer ! J'étais vraiment nul en maths à l'école et grâce à l'appli, je suis meilleur en maths ! Je suis tellement reconnaissante que vous ayez créé cette application.
Greenlight Bonnie
utilisateur Android
PARFAIT 🌟 💕🔥 ça facilite Vrmt la révision avec des fiches de révisions fascinants✨🥰
Khady
utilisatrice d'Android
Je conseille vraiment ! je galère à avoir des cours clairs et ça aide énormément !!
Claire
utilisatrice iOS
LES QUIZ ET CARTES MÉMOIRE SONT TROP UTILES ET J'ADORE Knowunity IA. C'EST LITTÉRALEMENT COMME CHATGPT MAIS EN PLUS INTELLIGENT !! ÇA M'A AIDÉ AVEC MES PROBLÈMES DE MASCARA AUSSI !! AINSI QUE MES VRAIES MATIÈRES ! ÉVIDEMMENT 😍😁😲🤑💗✨🎀😮
Raoul
utilisateur IOS
Knowunity est vraiment une application incroyable elle est pour tous les âges et s’adapte à tous les niveaux.Elle permet de mieux comprendre et apprendre. Cette application est super pour les devoirs et pour les contrôles je la recommande à tous le monde petit ou grands
Ella
utilisatrice iOS